Die Gebrauchstauglichkeit von Medizinprodukten ist ein zentraler Bestandteil der Patientensicherheit und regulatorischen Zulassung. Im Rahmen des Usability Engineering Prozesses nach IEC 62366-1 unterstützen wir Hersteller in der Medizintechnik, anwendungsbedingte Risiken systematisch zu identifizieren, zu bewerten und zu minimieren.
Von der Use Specification über formative Evaluationen bis hin zur summativen Validierung begleiten wir Sie strukturiert, normkonform und praxisnah – abgestimmt auf Ihr Produkt, Ihre Zielgruppen und Ihre MDR-Strategie.
USE-Ing. unterstützt Sie bei der nutzerzentrierten und MDR-konformen Entwicklung Ihrer Medizinprodukte.
Usability Engineering für Medizintechnik ist weit mehr als ein Usability-Test. Für Medizinprodukte ist es ein regulatorisch geforderter Prozess zur systematischen Identifikation und Minimierung anwendungsbedingter Risiken gemäß IEC 62366-1. Mängel in der Gebrauchstauglichkeit können nicht nur die Patientensicherheit gefährden, sondern auch zu Verzögerungen im Zulassungsprozess, zusätzlichen Studien oder kritischen Rückfragen durch Benannte Stellen führen. Ein strukturiert und normkonform umgesetzter Usability Engineering Prozess schafft Sicherheit – technisch, regulatorisch und wirtschaftlich.
Das Ergebnis: belastbare Usability-Nachweise für Benannte Stellen, reduzierte Design-Iterationen und beschleunigte Zulassungsprozesse.
Reduzierung regulatorischer und anwendungsbedingter Risiken
Vermeidung kostspieliger Design-Iterationen & Nachforderungen
Belastbare Validierung gegenüber Benannten Stellen & Behörden
Strukturierte Vorbereitung für effiziente Zulassungsprozesse
Erhöhte Patientensicherheit & nachhaltige Marktakzeptanz
Eine Analyse des medizintechnischen Nutzungskontextes (Context of Use Analysis) stellt den ersten Schritt des nutzerzentrierten Entwicklungsprozesses dar. Das Ziel: Eine Use Specification, welche zukünftige Benutzer (User), deren Aufgaben, Arbeitsabläufe (Tasks) sowie die Arbeitsumgebungen (Use Environments) systematisch und umfassend erfasst. In Übereinstimmung mit normativen Anforderungen, der IEC 62366-1 und weiteren Normen setzen wir zur Datenerhebung geeignete Methoden ein:
Je nach Projektanforderungen wählen wir das geeignete Verfahren. Durch Protokolle, Audio- und Videoaufzeichnungen bis hin zu fortschrittlichen Analysetools wie Eye-Tracking und Motion-Tracking erheben wir dabei alle relevanten qualitativen und quantitativen Daten. In der anschließenden Anforderungsanalyse leiten unsere Experten die relevanten User Requirements und User Needs.
Möchten Sie Ihre Benutzer wirklich verstehen und somit echten Nutzen schaffen?
Wir unterstützen Sie dabei.
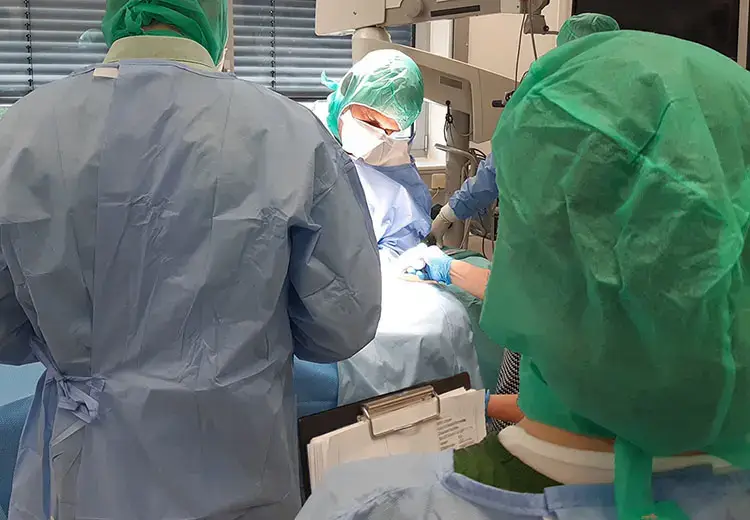

Wir helfen Ihnen bei der Analyse und Minimierung potenzieller Risiken der Produktnutzung. Die ISO 14971 verpflichtet im Rahmen der Entwicklung von Medizinprodukten dazu. Unsere Experten berücksichtigen dabei interaktions- und nutzungsbedingte Risiken (Use-related Risks) sowie gefährliche Situationen (Hazardous Situations) und definieren anwendungsbezogene Gefahrenszenarien (Hazard-related Use Scenarios) für Sie. Um diese kritische Usability-Engineering-Phase erfolgreich abzuschließen, unterstützen wir Sie daher mit:
Unsere Erfahrung bei Planung, Durchführung und Auswertung erleichtert dabei die Integration in die technische Risikobewertung.
Wollen Sie zuverlässig eine sichere Anwendung Ihres Medizinprodukts gewährleisten?
Wir kümmern uns darum.
Im Rahmen der Spezifikation werden die in der Analyse erhobenen Informationen gebündelt. Dies geschieht auf Anforderungsebene durch die Ableitung von Nutzungsanforderungen und User Interface Requirements, die in Form eines Lasten- und Pflichtenhefts gebündelt und spezifiziert werden können. Anhand von Workflow-Analysen werden Aufgabenmodelle (Tasks) erarbeitet und in regulatorisch notwendige Nutzungsszenarien (Use Scenarios) transferiert. Aber auch die Erarbeitung eines regulatorisch relevanten Nutzungsspezifikationsdokuments (Use Specification) lässt sich hierunter fassen. Das Resultat: Stärken und Schwächen des Medizinproduktes und des Workflows werden sichtbar und können durch intelligente Produktgestaltung optimiert werden.
Sie fragen sich, wie sich die Lücke zwischen qualitativer Forschung und technischer Spezifikation schließen lässt?
Unsere Experten unterstützen Sie bei der Entwicklung Ihrer Anforderungsspezifikation.

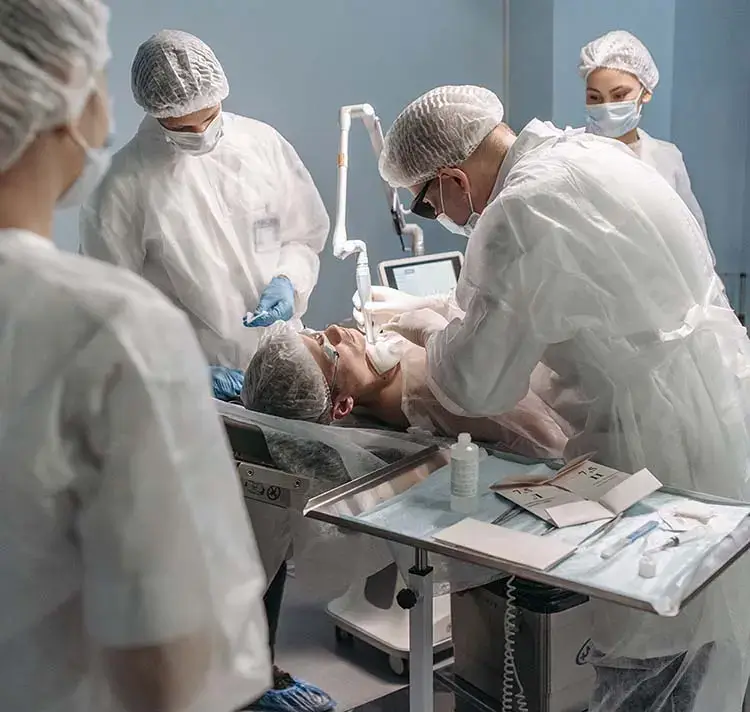
Sowohl die FDA Guideline als auch die IEC 62366-1 sehen die Absicherung der Usability, sowohl entwicklungsbegleitend (formativ) als auch entwicklungsabschließend (summativ), durch den gezielten Einsatz von Usability Evaluationsmethoden vor. Unsere Experten führen sowohl expertenbasierte Inspektionsmethoden, wie den Cognitive Walkthrough oder Heuristische Evaluationen, als auch Usability Tests mit Probanden durch oder unterstützen Sie bei den Ihrigen. Die Rekrutierung repräsentativer Testnutzer stellt dabei einen wichtigen und regulatorisch verpflichtenden Faktor dar. Mit unserem Probandenpool von über 3000 medizinischen Fachkräften sind wir in der Lage, jede medizinische Fachdisziplin abzubilden und für Tests zu rekrutieren. Die normgerechte Auswertung und verständliche Aufbereitung der Studienergebnisse gehören selbstverständlich ebenso zu unserem Repertoire.
Sie möchten die Gebrauchstauglichkeit Ihrer Medizinprodukte vor Inverkehrbringung mit medizinischen Fachanwendern testen?
Wir freuen uns darauf, Sie zu unterstützen.
Wir unterstützen Hersteller von Medizinprodukten bei der sicheren und effizienten Umsetzung des Usability Engineering Prozesses – von der Kontextanalyse bis zur summativen Validierung.
Sicherere Medizinprodukte entwickeln durch ein systematisches Usability-Engineering-Verfahren.
Wie man IEC 62366-1 erfolgreich anwendet: praktische Strategien zur Beschleunigung der Zulassung, Minimierung von Anwendungsfehlern und Erhöhung der Patientensicherheit.
Warum das wichtig ist

Certified Medical Devices Usability Expert (TÜV)
UXQB® Certified Professional for Usability and User Experience (CPUX-F)
Apelvo ist ein app-basiertes Trainingssystem der Firma Fysor für Beckenbodentraining mit spielerischen Elementen. Ziel des User…

Das interaktive Online-Training für Fachkräfte mit Schwerpunkt auf dem regulatorischen Human-Factors- und Usability-Engineering-Prozess für Medizinprodukte. Mit der Möglichkeit, das CPUX-F-Zertifikat zu erwerben.
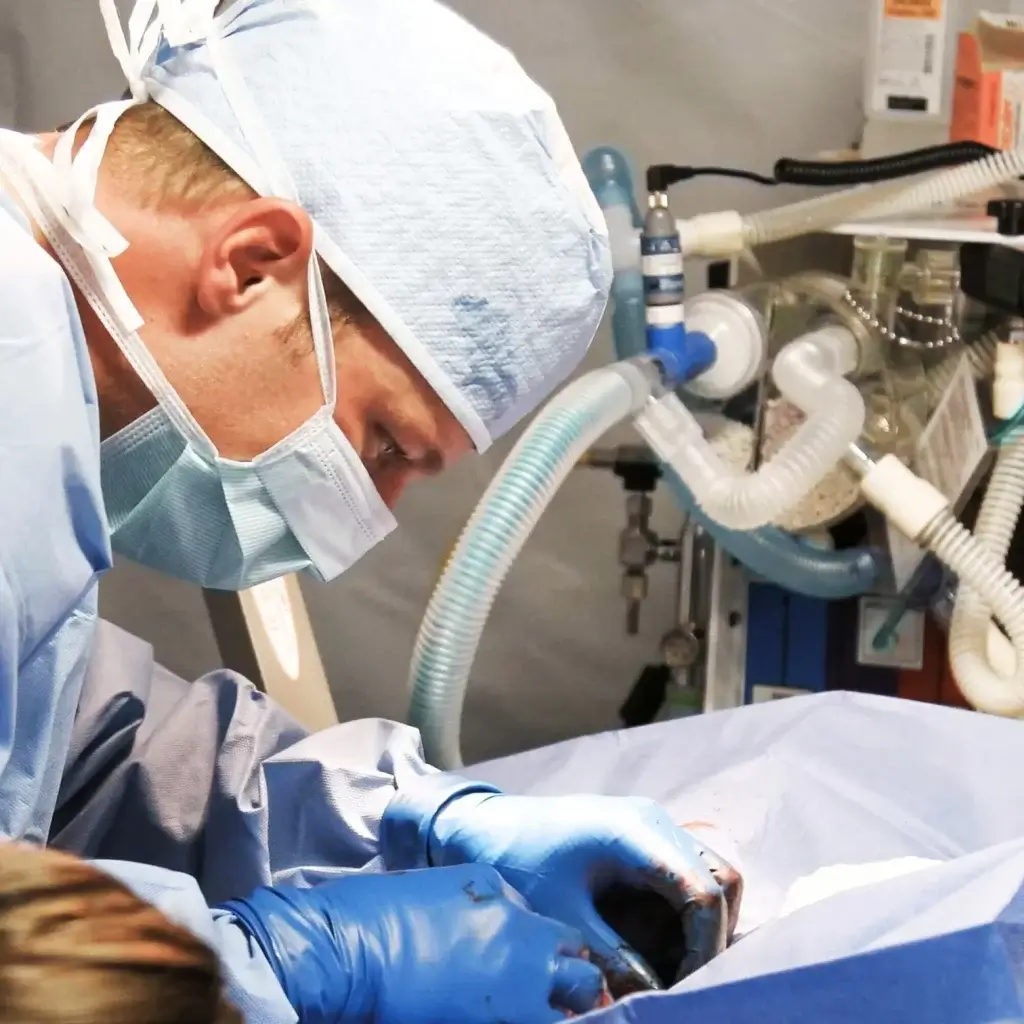
In diesem FAQ beantworten wir die wichtigsten Fragen zum Usability Engineering für Medizinprodukte, zu regulatorischen Anforderungen gemäß IEC 62366-1 sowie zur praktischen Umsetzung im Entwicklungsprozess.
Usability Engineering für Medizinprodukte ist ein normativ geregelter Prozess zur Identifikation und Minimierung anwendungsbedingter Risiken. Er ist in der IEC 62366-1 definiert und verlangt eine systematische Analyse von Nutzungskontext, User Interface, möglichen Use Errors und deren Risikobewertung. Ziel ist es, die Gebrauchstauglichkeit nachweislich sicherzustellen und Patientensicherheit sowie regulatorische Konformität zu gewährleisten.
Usability Engineering sollte bereits in der frühen Konzept- und Definitionsphase eines Medizinprodukts beginnen. Die IEC 62366-1 fordert eine systematische Analyse des Nutzungskontexts, bevor Designentscheidungen finalisiert werden. Eine frühzeitige Integration ermöglicht es, anwendungsbedingte Risiken bereits in der Konzeptphase zu identifizieren und zu reduzieren.
Werden Usability-Aktivitäten erst kurz vor der Zulassung durchgeführt, steigt das Risiko kostenintensiver Designänderungen oder zusätzlicher Validierungsstudien. Aus regulatorischer Sicht ist es daher sinnvoll, Usability Engineering parallel zum Risikomanagement nach ISO 14971 von Beginn an einzuplanen.
Ja. Die EU-MDR (Medical Device Regulation) fordert die Berücksichtigung von Gebrauchstauglichkeit und anwendungsbedingten Risiken. Die praktische Umsetzung erfolgt in der Regel über den Usability Engineering Prozess gemäß IEC 62366-1 in Verbindung mit dem Risikomanagement nach ISO 14971. Ohne diesen Nachweis ist die Konformitätsbewertung durch Benannte Stellen gefährdet.
Eine summative Usability-Validierung ist erforderlich, wenn das finale oder nahezu finale Design eines Medizinprodukts überprüft werden muss. Ziel ist der Nachweis, dass keine inakzeptablen anwendungsbedingten Risiken verbleiben. Sie ist ein verpflichtender Bestandteil des Usability Engineering Prozesses nach IEC 62366-1 und wird vor Einreichung bei Benannten Stellen durchgeführt.
Die IEC 62366-1 schreibt keine feste Anzahl an Testpersonen vor. Stattdessen fordert sie eine ausreichende Repräsentativität der vorgesehenen Anwendergruppen. Die Anzahl der Probanden hängt von Risikoklasse, Nutzungsszenario und Komplexität des Produkts ab. In der Praxis orientieren sich viele Validierungsstudien an regulatorischen Erfahrungswerten und FDA-Guidelines.
Die Usability Engineering File (UEF) dokumentiert alle Schritte des Usability Engineering Prozesses. Dazu gehören die Use Specification basierend auf einer Nutzungskontextanalyse, die Identifikation von Use Errors und deren Überführung in Hazard-related Use Scenarios, Nutzungsrisikobewertungen sowie die Dokumentation der formativen und summativen Evaluationen. Die UEF dient als Nachweis gegenüber Benannten Stellen und Behörden.
Die formative Evaluation dient der iterativen Optimierung des Designs während der Entwicklung. Die summative Evaluation hingegen validiert das finale Produkt hinsichtlich sicherer und wirksamer Anwendung. Beide sind Bestandteile des Usability Engineering Prozesses nach IEC 62366-1, verfolgen jedoch unterschiedliche Ziele.
Usability Engineering ist eng mit dem Risikomanagement nach ISO 14971 verknüpft. Anwendungsbedingte Risiken müssen identifiziert, bewertet und reduziert werden. Die Ergebnisse aus Nutzungskontextanalyse und Usability-Tests fließen direkt in die Risikobewertung ein und sind integraler Bestandteil der technischen Dokumentation.
In Europa prüfen Benannte Stellen im Rahmen der MDR die Umsetzung des Usability Engineering Prozesses. In den USA bewertet die FDA Human Factors und Usability Engineering im Rahmen von 510(k)- oder PMA-Verfahren. Auch andere internationale Behörden fordern entsprechende Nachweise.
Die Kosten einer Usability-Validierung für Medizinprodukte hängen von Produktkomplexität, Risikoklasse und Anzahl der vorgesehenen Anwendergruppen ab. Einflussfaktoren sind unter anderem der Umfang der Nutzungsszenarien, die Anzahl der Testpersonen, die Studiendurchführung (vor Ort oder remote) sowie der erforderliche Dokumentationsaufwand gemäß IEC 62366-1.
Bei höherklassigen oder besonders komplexen Medizinprodukten steigt der Aufwand für Planung, Rekrutierung und Auswertung entsprechend. Eine frühzeitige Abstimmung des Studiendesigns hilft, regulatorische Anforderungen effizient zu erfüllen und unnötige Zusatzkosten zu vermeiden.
